【Angew.Chem.】 15%的存活率与2倍的免疫增强:科学家打造“双密钥”纳米炸弹,精准爆破癌细胞司令部,让转移性乳腺癌无处遁形
✨文章标题:A Dual-Key Gated Nuclear-DNA-Targeted Photogenerator for Amplified Photodynamic Immunotherapy of Breast Cancer ✉️作者:Hongping Zhou 等 🔗链接:https://doi.org/10.1002/anie.202523661
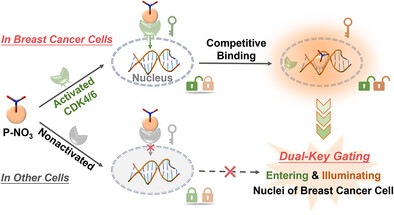
[!summary]
1. 研究背景与挑战:
乳腺癌是女性癌症死亡的主要原因之一。直接破坏癌细胞的核DNA是根治转移性乳腺癌的关键,但面临两大障碍:一是核膜这道天然屏障极难穿透;二是进入核内后如何实现高亲和力的精准定位,以及在肿瘤缺氧环境下如何保持杀伤力。
2. 核心技术创新( 系统的设计):
研究团队构建了一种名为 的酶介导光发生器,其核心在于双密钥(Dual-Key) 门控机制:
第一把密钥(穿膜): 分子结构中包含对称的吡啶酮单元,它能特异性地与乳腺癌细胞中过度激活的 CDK4/6 酶结合。这就像雇佣了细胞内的“内线”,通过主动运输方式穿过核孔复合体(NPC),规避了核膜的物理阻碍。
第二把密钥(锚定): 进入核内后,其带正电的吡啶基团通过强静电作用与带负电的 DNA 结合(结合能达 ),像锚一样精准锁定在 DNA 链上。
3. 杀伤机制(光动力免疫治疗):
DNA 作为能量放大器: 有趣的是,DNA 不仅仅是攻击目标,还充当了“电子储水池”。在光照下,DNA 能加速光发生器的电子转移,产生极高毒性的羟基自由基()。
无视缺氧: 这种 的生成可以通过水氧化路径实现,不依赖氧气,完美解决了肿瘤核心部位缺氧导致的治疗失效问题。
诱导系统免疫: 核 DNA 的原位破坏引发了基因崩塌(DD12, KDM4D, RGCC 等基因表达上调),释放损伤相关分子模式(DAMPs,如 HMGB1 和 CRT)。这不仅杀死了原发肿瘤,还激活了全身免疫反应,通过增加 T 细胞和抑制 Treg 细胞,实现了对远端转移瘤的清除。
4. 实验数据亮点:
高选择性: 仅在 CDK4/6 高表达的乳腺癌细胞(MCF-7, 4T1)中富集,在正常细胞或其他癌细胞中基本不进入核。
显著药效: 在 浓度及光照下,细胞存活率降至 15%;小鼠实验中,原发肿瘤彻底消退,远端转移瘤受到显著抑制。
免疫增强: 免疫因子(IL-12, TNF-, IFN-)水平提升 2 倍以上,免疫抑制细胞(Tregs)下降约 3 倍。
从“痛点”到“突破”:乳腺癌治疗为何总在“敲门”却进不去?
在现代医学的版图上,乳腺癌始终是一个令人谈之色变的对手,它不仅是全球女性恶性肿瘤致死的主要原因之一,更以其极高的转移率和复发率让无数家庭陷入绝望 。尽管我们已经开发出了手术、化疗、放疗以及新兴的免疫治疗等多种“武器库”,但面对那些已经扩散到远端器官的转移性乳腺癌,现有的疗法往往显得有些力不从心 。
科学界公认,要彻底摧毁癌细胞,最直接、最无解的方式就是捣毁它的“指挥中心”——细胞核 。细胞核内的DNA承载着生命的所有遗传蓝图,一旦DNA遭到不可修复的破坏,癌细胞的增殖和转移就会像断了线的木偶一样彻底崩溃 。然而,想要精准爆破这个“司令部”谈何容易?细胞核外包裹着一层致密且具有高度选择性的核膜,它像是一座戒备森严的堡垒,将绝大多数治疗药物拒之门外 。
即便一些幸运的药物通过分子扩散等方式进入了细胞核,它们往往也缺乏足够的“导航系统”去精准识别并锁定DNA长链,导致杀伤效率低下且极易产生副作用 。更糟糕的是,乳腺癌肿块内部通常处于严重的缺氧状态,而传统的光动力疗法高度依赖氧气来产生杀伤物质,这使得治疗在最需要它的肿瘤核心区域往往“哑火” 。
针对这些瓶颈,来自安徽大学、安徽农业大学等机构的研究团队在顶级期刊《德国应用化学》(Angewandte Chemie)上发表了一项颠覆性的研究。他们开发出了一种名为 的“双密钥”门控光发生器,通过一套巧妙的“入场券”系统和一种不依赖氧气的“爆炸”机制,成功实现了对乳腺癌及其转移瘤的精准打击,为攻克这一顽疾提供了前所未有的新思路 。
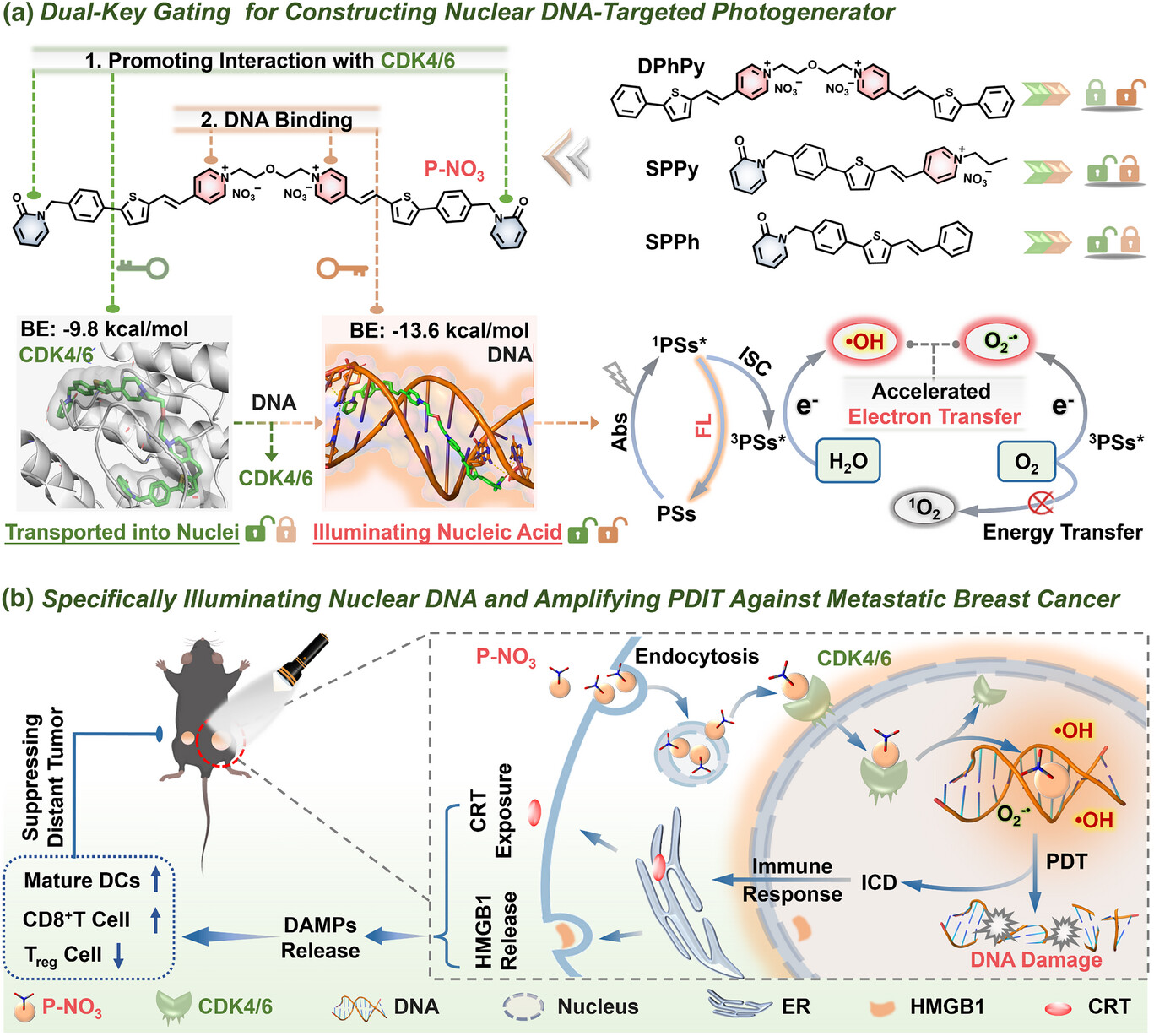
核心方法与技术细节:打造一枚会“特种作战”的分子导弹
这篇研究的核心魅力在于研究人员为 设计了一套近乎完美的“潜入与爆破”策略。为了让读者理解这个复杂的化学系统,我们可以将其类比为一场高科技的“斩首行动”。
第一把钥匙解决的是“如何潜入堡垒”的问题。研究人员敏锐地观察到,乳腺癌细胞的一个显著特征是细胞内的细胞周期蛋白依赖性激酶4和6(CDK4/6)处于高度过度激活的状态 。他们利用这一特性,在 分子的两侧安装了特殊的吡啶酮单元 。这些单元就像是伪造的“高级通行证”,能够特异性地吸引并诱导那些活跃的 CDK4/6 酶将药物包裹起来,通过主动运输的方式像“坐电梯”一样直接穿过戒备森严的核孔复合体,避开了核膜的阻碍 。分子模拟显示,这种结合能高达 ,确保了运输过程的稳定性和选择性 。
当这枚“导弹”成功潜入细胞核这个“司令部”后,第二把钥匙开始发挥作用,解决“如何精准定位”的问题。 分子中配备了带正电的吡啶基团,而细胞核内的 DNA 链天然带有负电荷 。基于这种“异性相吸”的原理,再加上吡啶基团对电子密集的碱基具有天生的“亲和力”, 能够像磁铁一样迅速且牢固地嵌入 DNA 的双螺旋结构中 。这种精准的锚定使得药物不再是核内游荡的散兵游勇,而是成为了贴在 DNA 核心部位的“定向炸弹”。
接下来是最具创新性的部分:爆破机制的升级。传统的治疗手段往往是在外围放火,寄希望于浓烟能熏死指挥官。而 选择在内部引爆。最精妙的一点是,它并没有自带“炸药”,而是将 DNA 本身转化为了“炸药”的一部分。DNA 链不仅是受攻击的目标,还是一个天然的“电子储水池” 。在特定波长的光照下, 与 DNA 之间会发生剧烈的电荷转移,利用周围的水分子通过“水氧化”路径直接产生毒性极强的羟基自由基() 。
这个过程不需要氧气的参与,这意味着即便是在氧气稀缺的肿瘤核心缺氧地带,这枚炸弹依然能爆发出惊人的威力 。这就好比开发出了一种能在真空环境中剧烈爆炸的新型火药,彻底解决了传统光动力疗法在肿瘤内部“水土不服”的世纪难题。通过这种“特种作战”模式,科研人员不仅让药物进得去,更让它打得准、爆得猛。
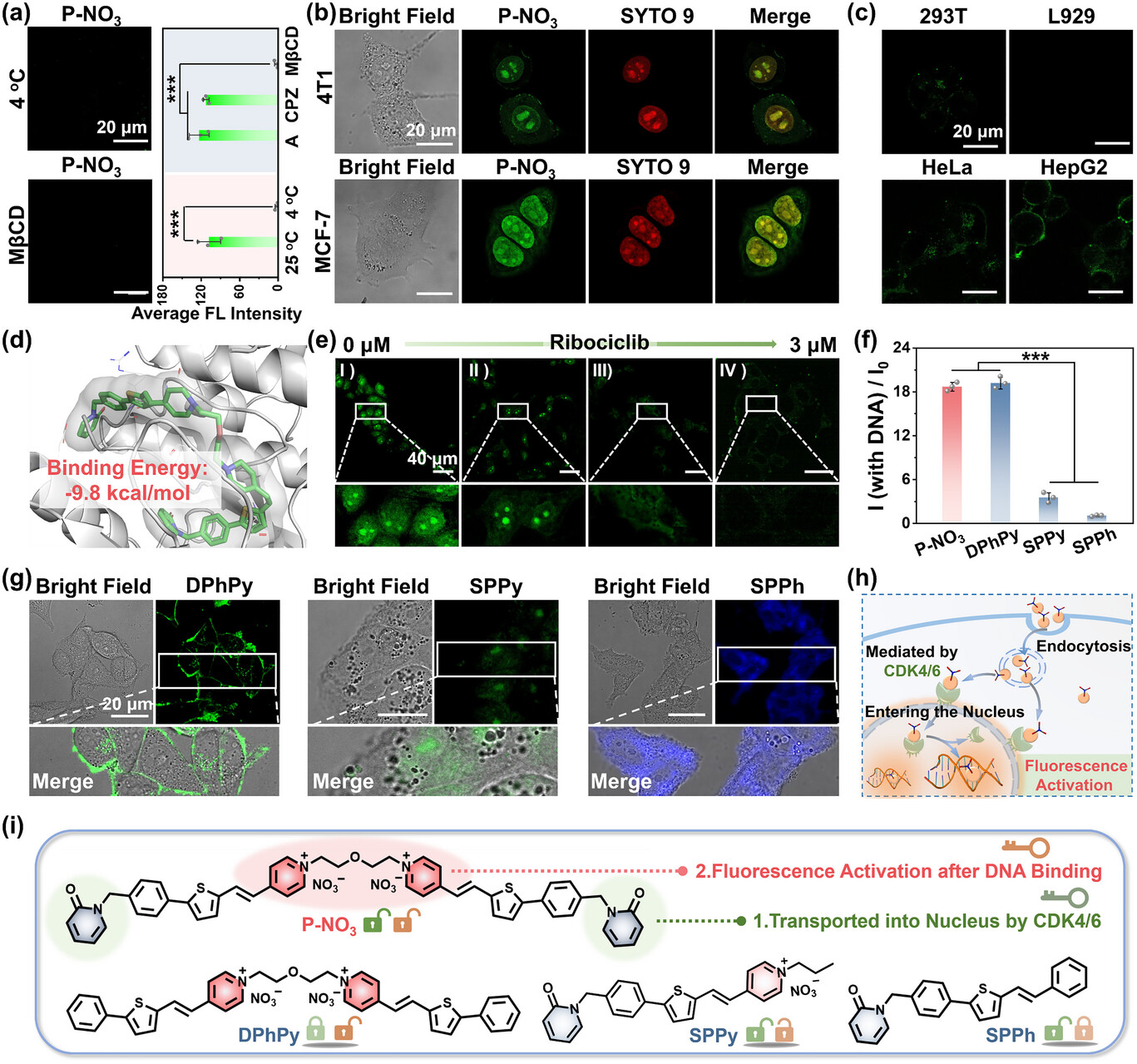
数据背后的创新与颠覆性:从细胞崩塌到全身免疫的奇迹
如果说设计思路是理想,那么实验数据就是支撑理想的硬道理。在这项研究中,一系列严谨的数据展示了 近乎压倒性的性能优势。
首先是针对“选择性”的极限测试。研究团队将 与几种缺乏“钥匙”的对照组分子(DPhPy、SPPy等)进行了对比观察 。实验结果令人震撼:只有具备完整“双密钥”结构的 能够在乳腺癌细胞核内产生强烈的荧光信号,并成功锁定 DNA 。在不表达 CDK4/6 的普通健康细胞或其他类型的癌细胞中,这种分子几乎无法进入核内,显示出了极高的生物安全性和精准度 。这意味着,我们可以在不伤害正常组织的前提下,对癌细胞进行“精确切除”。
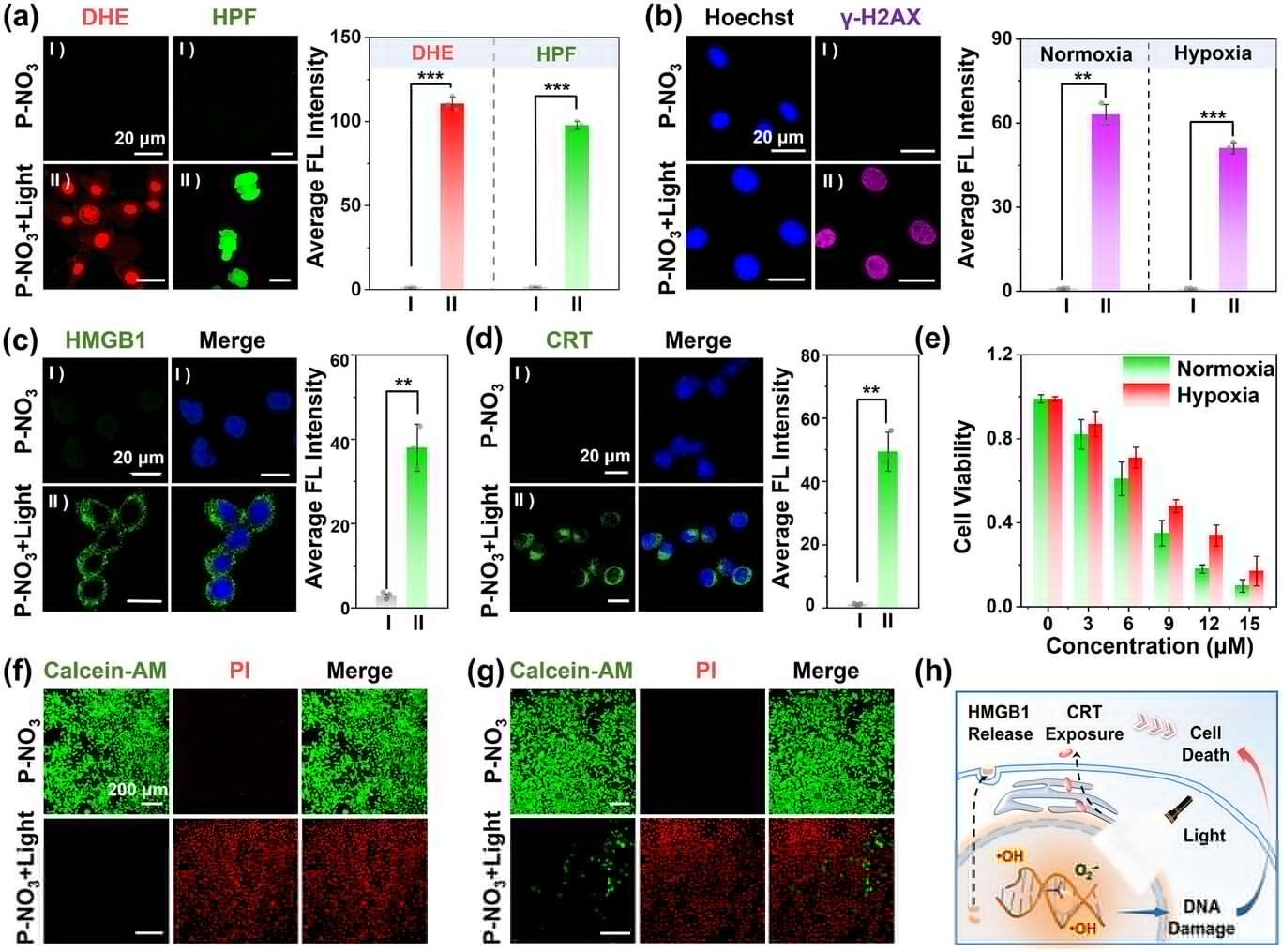
在杀伤效力方面, 展现出了摧枯拉朽的力量。在实验室环境下,当药物浓度仅为 时,配合短时间的光照,乳腺癌细胞的存活率竟然断崖式跌落至约 15% 。更值得注意的是,这种极高的杀伤率在常氧和模拟肿瘤的缺氧环境下几乎没有差别,这有力地证明了其“氧气无关型”爆破机制的可靠性 。
为了深入理解这种爆破是如何在基因层面起作用的,研究人员动用了昂贵的 RNA 测序技术。数据分析显示,在 治疗后,癌细胞内有 147 个基因显著上调,而 231 个基因被大幅抑制 。其中,负责 DNA 损伤响应和细胞凋亡的核心基因(如 DD12, KDM4D, RGCC 等)被强烈激活,而负责 DNA 修复的基因则被彻底“封杀” 。这意味着癌细胞在遭到轰炸后,不仅丧失了抵抗力,连自我修复的“维修部”也被一锅端了。
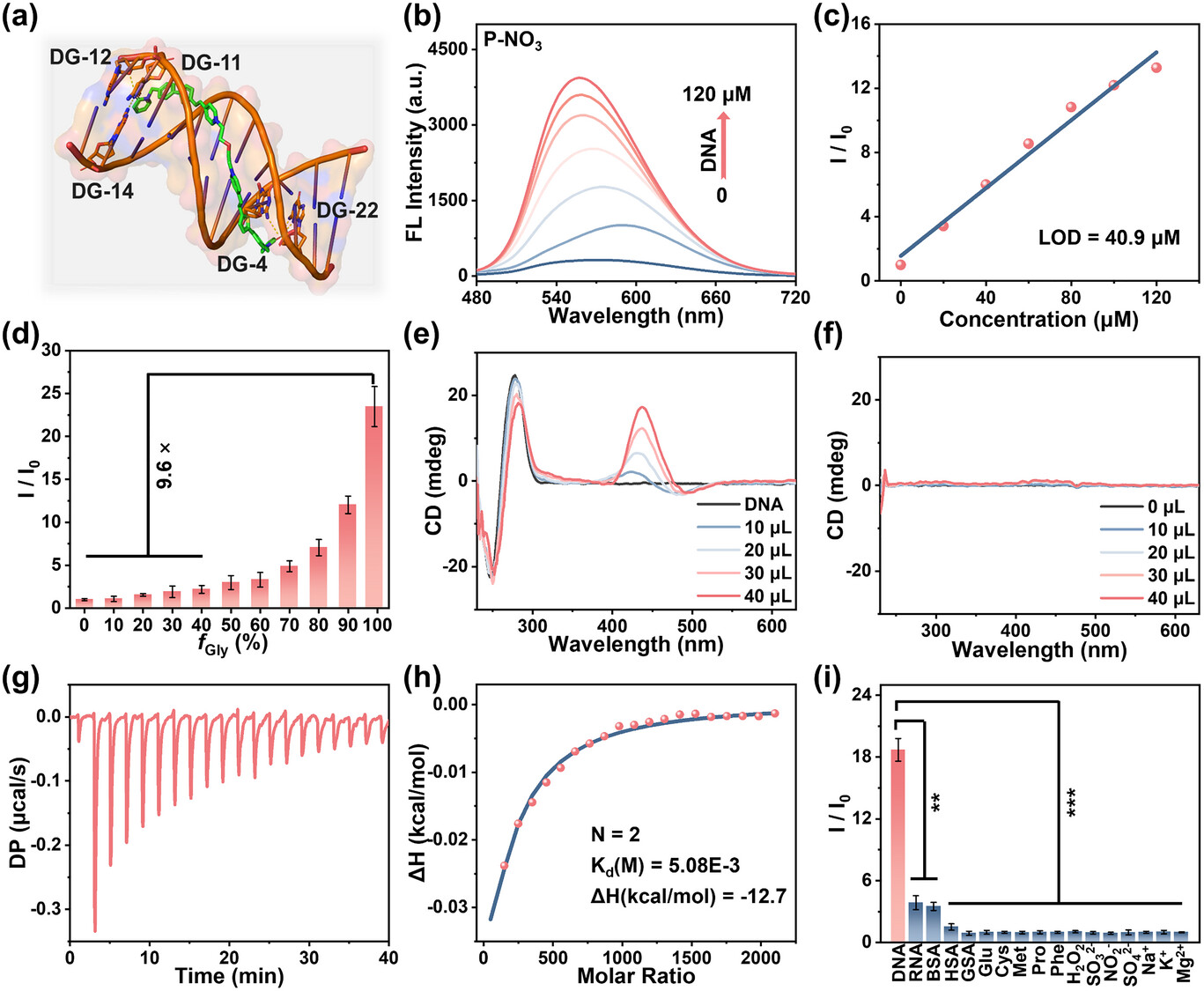
但最令人激动的突破还在后面:这种局部的爆破引发了全身性的“免疫风暴”。当 在核内撕碎 DNA 时,会诱导一种被称为“免疫原性细胞死亡(ICD)”的过程 。死亡的癌细胞会向外释放出大量的“危险信号”分子,包括高迁移率族蛋白 B1(HMGB1)和钙网织蛋白(CRT) 。这些分子就像是战场上的信号弹,瞬间吸引了免疫系统的注意。
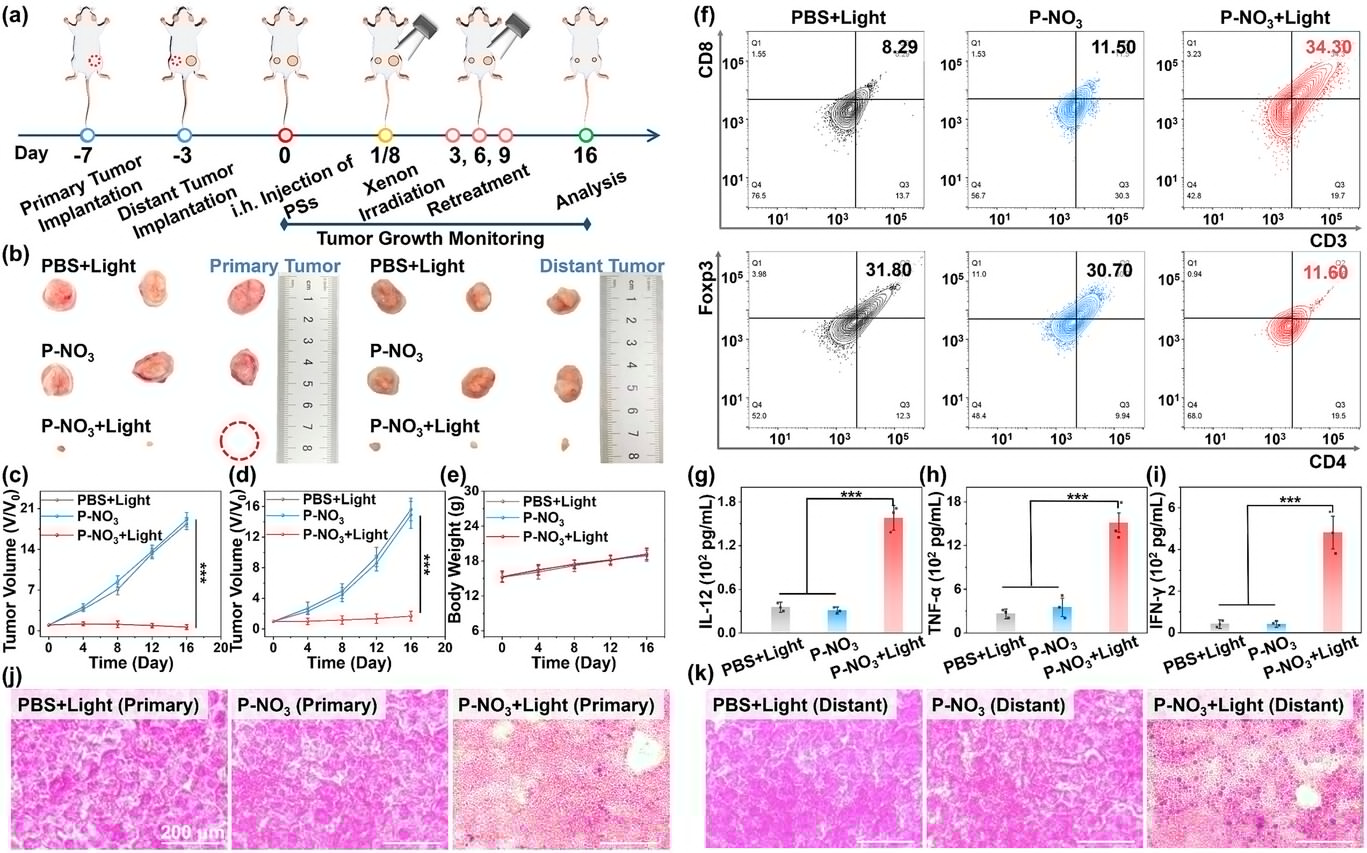
实验数据显示,在接受治疗的小鼠体内,血清中代表免疫激活强度的关键因子(如 IL-12, TNF-, IFN-)水平相比对照组提升了 2 倍以上 。与此同时,肿瘤内部负责杀伤敌人的 T 细胞(俗称“杀手 T 细胞”)的浸润比例增加了约 2 倍,而那些专门保护癌细胞、抑制免疫反应的调节性 T 细胞(Treg)的比例则骤降了约 3 倍 。
这种免疫环境的彻底逆转,产生了一个堪称医学奇迹的效果:研究人员在小鼠身上同时建立了“原发肿瘤”和“远端转移瘤”模型。在对原发瘤进行光照治疗后,不仅受照部位的肿瘤被彻底清除( eradicatied ),那些并未受到光照、位于身体远端的转移瘤竟然也出现了明显的退缩和抑制 。这证明了 成功地将一个局部的物理治疗转化为了一个全身性的免疫治疗,实现了“一处爆破,全线溃败”的宏大效果。相比于目前临床上效果有限且副作用巨大的系统性化疗,这种局部激活、全局响应的模式无疑具有降维打击的优势。
应用展望、局限性与未来路线图:通往“治愈”的最后一公里
尽管 在动物实验中表现出了令人咋舌的潜力,但作为严谨的科学传播者,我们必须清醒地看到,从实验室走向临床依然面临挑战。目前的局限性主要在于,实验所用的光照穿透深度仍有限,这对于皮肤表层或浅层组织的乳腺癌效果极佳,但对于深埋在体内的深部肿瘤,可能需要结合内窥镜技术或开发波长更长、穿透力更强的光敏系统。
此外,尽管该分子在小鼠模型中显示了极佳的生物安全性,但在人体内长期的代谢路径和潜在的蓄积毒性仍需通过更加严格的临床前研究来验证。未来的研究路线图已经非常清晰:一方面是优化分子结构,使其能响应能量更低、穿透力更强的近红外光;另一方面是探索其在除乳腺癌外、其他同样具有 CDK4/6 高表达特征的癌症(如部分肺癌、卵巢癌)中的普适性。
总的来说,这项“双密钥”研究不仅提供了一个高效的抗癌工具,更重要的是,它为我们展示了一种全新的设计哲学:与其费力地对抗生物屏障,不如“借力打力”,利用癌细胞自身的激酶作为向导,利用其自身的 DNA 作为能量源。随着这种精准医疗技术的不断迭代,我们有理由相信,在不远的未来,转移性乳腺癌将不再是一个死刑判决,而是一个可以被精准爆破、从基因层面彻底抹除的“小手术”。这场关于生命与微观粒子的较量,正以前所未有的速度迈向胜利。